破解临床困境,我国专家为“沉默肿瘤”绘制全球首张全景图谱
- 房产
- 2025-04-04 11:40:06
- 3
4月4日,澎湃新闻(www.thepaper.cn)记者从复旦大学附属肿瘤医院获悉,该院院长虞先濬教授团队联合北京大学肿瘤医院、中国科学院上海药物研究所、上海长海医院、中国科学院分子细胞科学卓越创新中心,历时五年研究,成功绘制全球首张无功能性胰腺神经内分泌瘤多组学全景图谱,并根据图谱突破性提出这种“沉默肿瘤”的分子分型框架、预后模型和靶向-免疫治疗新策略,为临床精准诊疗提供了重要依据。国际顶级肿瘤学期刊《癌细胞》(Cancer Cell)同日发表该项重要研究成果,影响因子为48.8分。
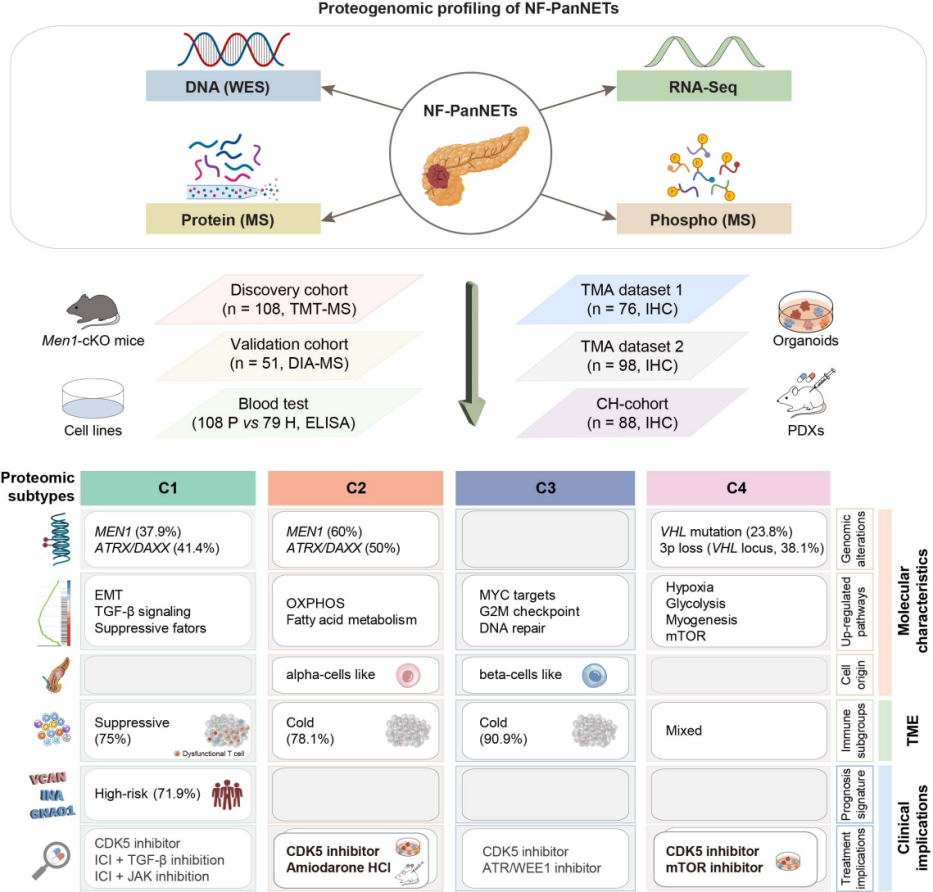
虞先濬教授团队联合北京大学肿瘤医院、中国科学院上海药物研究所、上海长海医院、中国科学院分子细胞科学卓越创新中心,历时五年研究,成功绘制全球首张无功能性胰腺神经内分泌瘤多组学全景图谱。复旦大学附属肿瘤医院 供图
历时5年攻关,绘制出全景分子图谱
神经内分泌肿瘤起源于神经内分泌细胞,这种细胞遍布人体各处,胃、肠、胰腺等消化系统最常见,在我国患者中发生在胰腺部位的最多。
胰腺神经内分泌瘤是发生在胰腺的第二大常见肿瘤,约90%为无功能性。这类无功能性胰腺神经内分泌瘤早期没有症状,因而也被称作“沉默的肿瘤”。其中约半数患者确诊时已发生转移,特别是肝转移,且接受根治手术后也有不少患者容易复发,在临床上缺乏有效预测预后的分子标志物,综合治疗疗效有待提高。
历时五年攻关,虞先濬教授团队联合多中心研究团队,整合基因组、转录组、蛋白质组和磷酸化修饰组四种组学数据,绘制了全球首个无功能性胰腺神经内分泌瘤蛋白基因组学全景分子图谱。
团队通过对108例中国无功能性胰腺神经内分泌瘤患者开展全外显子组、转录组、蛋白质组及磷酸化修饰组的多维度整合分析,绘制出全景分子图谱,揭示了MEN1、ATRX、DAXX基因突变通过干扰染色质结构稳定性和激活mTOR通路驱动肿瘤恶性演进的机制。
研究团队还通过MEN1基因条件性敲除小鼠模型,验证了MEN1缺失触发代谢重编程和增殖信号交叉激活的恶性循环,从而导致染色体分离至关重要的CENPV蛋白下调,填补了该领域机制研究的空白。另外,CDK5、WASL等基因的拷贝数扩增被发现为无功能性胰腺神经内分泌瘤生长的驱动因素,有望成为靶向治疗的潜在“靶标”。
筛选“靶标”建立预后模型,有效预测患者生存预后
研究团队发现,在无功能性胰腺神经内分泌瘤患者的临床诊疗中,传统肿瘤分期及病理分级难以满足个体化治疗的需求。
为了解决这一临床困境,研究团队基于海量蛋白质组数据,利用前期研发的ReProMSig 平台基于人工智能算法筛选出GNAO1、INA、VCAN三个蛋白质,构建了预后标志物特征谱和预后模型,为无功能性胰腺神经内分泌瘤的预后判断提供了重要工具。
据介绍,该模型在包含345例患者的四组独立队列中均展现出优良的预测效能和区分效果:高危患者五年生存率仅为51.4%,而低危组则高达97.8%。更具临床意义的是,研究团队还证实分泌蛋白VCAN在患者血浆中的浓度与肿瘤进展显著相关,这一发现有望推动诊疗模式从“有创组织活检”向“无创血液检测”跨越。
与此同时,研究团队进一步通过蛋白质组学特征聚类分析,将无功能性胰腺神经内分泌瘤患者划分为四种分子亚型。其中,C1亚型的肿瘤以免疫抑制微环境和EMT通路激活为特征,患者预后最差,急需探索免疫联合疗法;C2亚型表现出异常活跃的氧化磷酸化活性; C3亚型由MYC 异常激活和失控的细胞周期信号主导;C4亚型则在VHL突变驱动下形成独特的缺氧生态。
研究团队后续的药物研究证实了“四分型”的准确性。基于各亚型特异激活的蛋白激酶和表达和活性上调蛋白,团队利用患者来源类器官(PDO)开展了药物筛选并利用患者来源肿瘤异种移植模型(PDX)进行验证,证实CDK5抑制剂可抑制四种分子亚型的肿瘤生长;钙离子通道阻滞剂(如心血管疾病经典药物盐酸胺碘酮)与 CDK5 抑制剂两药联用在C2亚型中表现出更好的抑瘤效果;目前临床运用的mTOR 抑制剂可较好抑制C4 亚型肿瘤。这些证据显示,基于“四分型”的“分型而治”策略,为个体化精准治疗提供了科学依据。
上一篇:快速估算基金净值的方法















有话要说...